 用药反馈
用药反馈
点击下载《本维莫德乳膏治疗银屑病专家指导意见》完整版PDF 提取密码:ecs3
中国皮肤性病学杂志
TheChineseJournalofDermatovenereology
ISSN1001-7089,CN61-1197/R
《中国皮肤性病学杂志》网络首发论文
题目: 本维莫德乳膏治疗银屑病专家指导意见
作者: 张学军,中华医学会皮肤性病学分会银屑病学组
DOI: 10.13735/j.cjdv.1001-7089.202103186
收稿日期: 2021-03-30
网络首发日期: 2021-05-11
引用格式:张学军,中华医学会皮肤性病学分会银屑病学组.本维莫德乳膏治疗银屑病专家指导意见.中国皮肤性病学杂志.
https://doi.org/10.13735/j.cjdv.1001-7089.202103186
网络首发:在编辑部工作流程中,稿件从录用到出版要经历录用定稿、排版定稿、整期汇编定稿等阶段。录用定稿指内容已经确定,且通过同行评议、主编终审同意刊用的稿件。排版定稿指录用定稿按照期刊特定版式(包括网络呈现版式)排版后的稿件,可暂不确定出版年、卷、期和页码。整期汇编定稿指出版年、卷、期、页码均已确定的印刷或数字出版的整期汇编稿件。录用定稿网络首发稿件内容必须符合《出版管理条例》和《期刊出版管理规定》的有关规定;学术研究成果具有创新性、科学性和先进性,符合编辑部对刊文的录用要求,不存在学术不端行为及其他侵权行为;稿件内容应基本符合国家有关书刊编辑、出版的技术标准,正确使用和统一规范语言文字、符号、数字、外文字母、法定计量单位及地图标注等。为确保录用定稿网络首发的严肃性,录用定稿一经发布,不得修改论文题目、作者、机构名称和学术内容,只可基于编辑规范进行少量文字的修改。
出版确认:纸质期刊编辑部通过与《中国学术期刊(光盘版)》电子杂志社有限公司签约,在《中国学术期刊(网络版)》出版传播平台上创办与纸质期刊内容一致的网络版,以单篇或整期出版形式,在印刷出版之前刊发论文的录用定稿、排版定稿、整期汇编定稿。因为《中国学术期刊(网络版)》是国家新闻出版广电总局批准的网络连续型出版物(ISSN2096-4188,CN11-6037/Z),所以签约期刊的网络版上网络首发论文视为正式出版。
网络首发时间:2021-05-1110:57:03
网络首发地址:https://kns.cnki.net/kcms/detail/61.1197.R.20210511.0916.001.html
中华医学会皮肤性病学分会银屑病学组
[摘要]本维莫德乳膏是我国拥有完整自主知识产权的国家1类新药,对银屑病发病过程中的多个环节,包括抗炎、调节表皮角质形成细胞角化、减少真皮血管新生等具有调节作用,在轻中度寻常性银屑病治疗中具有良好疗效和安全性。为了科学有效的使用本维莫德乳膏治疗轻、中度斑块型银屑病,中华医学会皮肤性病学组召集相关专家制定本指导意见,以本维莫德的药理作用机制、治疗银屑病的临床试验结果以及针对毒副作用的动物实验结果为依据,目的为规范、合理、安全地使用本维莫德乳膏治疗银屑病。
[关键词]银屑病;本维莫德;治疗;指导意见[中图分类号]R758.63[DOI]10.13735/j.cjdv.1001-7089.202103186
(Psoriasis Research Group of Chinese Society Dermatology)
[Corresponding author] ZHANG Xuejun, E-mail ayzxj@vip.sina.com
[Abstract] Benvitimod, as a national class 1 new drug with complete and independent intellectual property rights in China, which has regulatory effect on the pathogenesis of psoriasis, such as anti-inflammatory, regulating epidermal keratinization and reducing angiogenesis, showing good curative response and safety for mild to moderate psoriasis vulgaris. In order Benvitimod cream to be used in scientifically and effectively for psoriasis treatment, the Psoriasis Group of Dermatology and Venereology Branch, Chinese Medical Association, convened relevant experts to formulate this consensus as the reference for domestic dermatologists. This consensus is d on the pharmacological mechanism, the clinical trial for psoriasis treatment, and the results of animal experiments aimed at toxic and side effects of benvitimod. The arm of this consensus is for standard, reasonable and safe use of benvitimod for psoriasis treatment.
[Key words] Benvitimod: Psoriasis; Treatment; Consensus
银屑病是一种慢性、复发性、炎症性疾病,主要由T淋巴细胞异常活化引起,目前无法治愈,需要长期管理。银屑病典型皮损为鳞屑性红色斑块,可伴有瘙痒、疼痛,病理上以角质形成细胞过度增殖伴角化不全、炎症细胞浸润和血管增生为主要特征。轻、中度寻常性银屑病最常用的外用药物包括皮质类固醇、维生素D3衍生物、煤焦油[1-2],但是停药后易复发、长期用药的安全性和耐药性等问题,使得新的非类固醇外用药的开发成为轻、中度银屑病患者迫切的治疗需求。本维莫德(Benvitimod)是一种非激素类、治疗性芳香烃受体(aryl hydrocarbon receptor,AHR)激动剂,从多个途径阻断银屑病的发病环节,且安全性较好。本维莫德乳膏是全球首创、拥有完整自主知识产权的国家1类新药,是我国“重大新药创制”科技重大专项成果,2019年5月在我国获批上市,用于成人轻、中度寻常性银屑病的局部治疗。本共识以本维莫德的药理作用机制、治疗银屑病的临床试验结果以及针对毒副作用的动物实验结果为依据,为规范、合理、安全地使用本维莫德乳膏治疗银屑病提出如下指导性建议。
1指导意见编制方法与过程本指导意见采用“文献研究法”、“专家共识会议法”制订。文献研究制定了检索文献的评价与纳排标准,以“本维莫德”、“苯烯莫德”、“Benvitimod”、“Tapinarof”、GSK2894512”、“WBI-1001”为关键词,检索的数据库包括PubMed、MEDLINE和Em、万方、知网、维普等,检索到截至2020年8月涉及该药的文献综述、随机和非随机对照临床试验、动物实验、基础研究等。通过标题、摘要以及全文阅读的方式,对获得文献进行筛选、去重、整理、归纳形成专家指导意见初稿;再以访谈、专家共识会议等方式对指导意见初稿进行修改,将共识度超过70%的意见予以采纳,重新整理形成指导意见论证稿,召开专家论证会进行研讨。根据专家意见进行反复修改,形成本指导意见。
本维莫德(Benvitimod),曾用名“苯烯莫德”,国外用名“Tapinarof”、“GSK2894512”、“WBI-1001”,-化学名为5-[(E)-2-苯乙烯基]-2-异丙基-1,3-苯二酚,化学结构式见图1,分子式C17H18O2,分子量为254.32。其分子内含2个苯环,苯环具有稳定性,不易分解,而其疏水基与亲水基则有利于分子进入组织中起作用,属于芪类小分子化合物[3]。
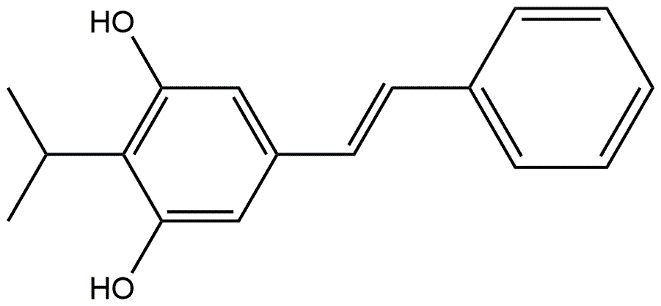
图1本维莫德化学结构式
Fig.1 Chemical structural formula of Benvitimod
2.1本维莫德的作用靶点 本维莫德是非激素类的治疗性芳香烃受体调节剂
(TAMA, therapeutic aryl hydrocarbon receptor modulating agent),可以特异性结合并激活芳香烃受体(AHR, aryl hydrocarbon receptor)发挥生物学效应[4]。AHR是一种可以感应多种内源性和外源性分子并影响多种生物学效应的细胞质配体激活转录因子,能够影响多种基因的转录及表达,具有诱导多种重要的外源性细胞色素P450酶(如CYP1A1、CYP1A2、CYP1B1等)作用,广泛存在于人体各组织细胞,近来被确定为天然和适应性免疫反应的关键调节器,在皮肤肿瘤、自身免疫性皮肤病、特应性皮炎、银屑病等疾病中发挥重要作用[5-8]。
AHR诱导Foxp3基因的表达[9],进而诱导Treg的生成,影响Th17和Treg细胞的平衡[6-8]。而Th17细胞因子(IL-17A、IL-17F和IL-22等)是银屑病发病过程中免疫失调的关键调控因子,驱动角质形成细胞过度增殖和趋化因子的产生,并持续募集白细胞[10,11]。AHR信号调控Th17细胞的终末分化以及IL-17、IL-22的表达,从而参与银屑病免疫应答。过多的中性粒细胞招募加重银屑病的炎症反应,AHR可负向调节中性粒细胞在炎症区域的招募,延缓银屑病病程进展[12]。AHR激活朗格汉斯细胞,进而抑制CD4+T细胞的增殖,提高免疫抑制因子IL-10的水平,增强免疫耐受[13]。银屑病患者表皮分化异常和皮肤屏障功能受损与皮肤屏障蛋白表达下调有关。AHR调节角质形成细胞终末分化,其激活和信号转导上调皮肤屏障蛋白基因的表达[14],促进皮肤屏障完整性,防止经表皮水分流失。此外,AHR介导的转录因子(如Nrf2)激活可调节抗氧化蛋白的表达,诱导细胞保护性抗氧化反应,从而抑制氧化应激并恢复皮肤稳态[8]。
2.2本维莫德的药理机制本维莫德通过激活AHR抑制Th17反应[15],从而针对银屑病发病的前炎症因子的过度表达、表皮细胞异常角化、血管新生以及免疫级联反应等环节起作用。局部使用本维莫德治疗咪喹莫特诱导银屑病样皮损的小鼠模型可以减轻皮肤炎症,并且呈剂量依赖的方式降低IL-17A、IL-17F、IL-19、IL-22、IL-23A和IL-1β的表达[8]。此外,本维莫德能够抑制炎症因子如IFN-γ、TNF-α、白细胞介素等的合成与释放,从而发挥抗炎作用。
银屑病的病理特点为表皮细胞增殖过快和角化不全,体外试验和动物体内试验表明本维莫德具有抑制表皮细胞增殖和诱导分化的作用[16],提示其可以通过针对银屑病发病机制中角质形成细胞异常的环节发挥治疗效应。本维莫德对普萘洛尔诱导豚鼠银屑病模型的病理改变有明显恢复作用,使其棘层变薄,表皮突下延程度减轻[16]。皮损血管增生和毛细血管扩张是银屑病皮损的显著特征,动物试验中还观察到本维莫德显著抑制新生血管形成以及微血管扩张的现象[16]。
活化T细胞介导的免疫级联反应导致皮肤炎症细胞浸润是银屑病皮损形成的重要环节。本维莫德可以诱导人外周血单个核细胞的早期凋亡和晚期凋亡;当本维莫德作用于活化的T细胞后,随着时间的延长,NF-κB通路中活化因子表达逐渐降低,而抑制性因子表达则逐渐升高[17],提示本维莫德可以通过负向调节T细胞NF-κB通路,进而调控T淋巴细胞介导的免疫级联反应。此外,本维莫德还可抑制STAT1磷酸化,促进皮肤屏障功能的修复[18]。
综上所述,本维莫德对银屑病的多个致病环节均有抑制作用,包括抑制前炎症因子的表达、直接对角质细胞的作用、抑制新生血管生成以及毛细血管扩张以及调控T细胞活化,从而发挥治疗作用。
本维莫德分子量较小,脂溶性较高,适用于局部用药。药代动力学研究结果显示,本维莫德乳膏局部吸收良好,系统吸收极低[19-21],在外用本维莫德患者的1232份血清样品中,仅47份(3.8%)检出本维莫德,且浓度很低(0.21~2.93ng/mL);多次给药也未见蓄积,与正常皮肤比较,银屑病皮疹对本维莫德的吸收并无明显变化。
3本维莫德乳膏治疗银屑病疗效证据
本维莫德乳膏制剂对于轻、中度斑块状银屑病有一定改善作用,是有效的外用抗炎分子[22-23]。随机、双盲、安慰剂对照的II期临床试验[23]评估了本维莫德乳膏治疗轻、中度斑块状银屑病患者(BSA<10%,PGA为2~3分)的有效性和安全性。分别使用本维莫德乳膏或安慰剂,每天早晚各一次,持续12周后,本维莫德组PGA改善率为62.8%,显著高于安慰剂组(13.0%,P<0.0001);本维莫德组达到PGA0/1的比率与BSA平均改善率分别为67.5%和79.1%,均显著高于安慰剂组(P<0.0001)。
国内已经完成了本维莫德乳膏治疗轻、中度银屑病多中心、随机、双盲、安慰剂、阳性药对照的III期临床试验[24]。受试者按照2:1:1的比例随机分3组,分别使用本维莫德乳膏、阳性对照药0.005%卡泊三醇软膏和安慰剂,每天早晚各一次,连续用药12周,停药后随访8周。从第2周开始,本维莫德组在各访视点的红斑、浸润/肥厚、鳞屑积分值小于安慰剂组(P<0.05)。治疗12周后,本维莫德组疗效优于卡泊三醇组和安慰剂组(P<0.05),三组的PASI75应答率分别为50.4%(本维莫德组)、38.5%(卡泊三醇组)、13.9%(安慰剂组);本维莫德组与卡泊三醇组的PGA的应答率分别为66.3%和63.9%,两组无显著差异,但均显著高于安慰剂组(33.5%,P<0.05)。对治愈病例进行为期8周随访,结果显示本维莫德组和卡泊三醇组复发率分别为7.3%和8.5%,各组被随访受试者复发时间差异无统计学意义(P>0.05)。
对III期临床试验中部分使用本维莫德乳膏治愈的患者进行了为期40周的长期用药临床研究,观察缓解时间、复发情况和有效性。结果显示,59例完成为期1年试验的受试者中30例(50.8%)复发。从治愈至复发的平均中位缓解期约为9个月。
4.1适应证 ①成年轻中度寻常性银屑病患者,对糖皮质激素和(或)维生素D3衍生物外用制剂不能耐受或疗效不满意者;②不能耐受系统药物治疗的成年中度寻常性银屑病患者;③成年中重度寻常性银屑病患者经系统药物治疗后皮损清除不满意者;④关节病型银屑病、局限性脓疱型银屑病患者可在知情同意及医师严格监控下谨慎使用。
4.2使用方法皮损局部外用,早晚各一次,均匀涂抹于患处,不建议用于头面部、口周及眼睑、腹股沟、肛门生殖器等部位。每日最大使用剂量不超过6g,治疗面积不应超过体表面积的10%。涂药后皮损避免紫外线照射。皮疹消退后可逐渐停药,停药后复发可再用。本药可与糖皮质激素、维生素D3衍生物等外用药物进行交替及序贯治疗。
4.3不良反应
Ⅲ期临床试验期间报告的本维莫德不良反应发生率高于安慰剂和卡泊三醇(P<0.001)。本维莫德最常见的不良反应是用药部位皮肤反应,主要包括用药部位瘙痒(最常见)、接触性皮炎、毛囊炎、角化性丘疹、疼痛、红斑、皮肤水肿、色素异常等,且均以轻中度为主;Ⅲ期试验期间报告的与本维莫德乳膏有关或可能有关的严重不良事件报告共2例,均表现为接触性皮炎。在用药部位皮肤不良反应中,角化性毛囊性丘疹是较为特征的表现,常见于躯干、四肢,其产生的机制可能因为AHR在人表皮、毛囊及皮脂腺上均有高表达,AHR激活可使毛囊皮脂腺单位的干细胞优先向表皮细胞分化,导致毛囊出现表皮样增生和角化过度,皮脂腺减少并逐渐被角化的表皮细胞取代[25],进而产生角化性毛囊性丘疹,因此不建议本维莫德乳膏应用于头面部。皮肤反应的程度呈剂量依赖性,本维莫德浓度增加表现出较高的累积刺激性评分[26]。不采取处理措施或调整用药剂量后症状可以消退。
系统性不良反应少见,临床试验期间观察到的系统不良事件包括感染(如流感、尿路感染、上呼吸道感染、鼻咽炎、发热、皮肤感染等)、转氨酶升高、腹泻、上腹痛、胸闷、哮喘、频发室早、频发房早等。研究者判断所有不良事件与外用本维莫德无关。
5.1 使用本维莫德乳膏的注意事项:①用药前应叮嘱患者本维莫德乳膏每日使用最大剂量不能超过6g,治疗皮损面积不应超过体表面积的10%;涂布药物后需避光;②嘱患者勿用于头面部、口周及眼睑、腹股沟、肛门生殖器等部位以及表面破损的皮肤,不可封包;③本维莫德临床试验为12周,连续使用超过12周的有效性以及安全性尚未确立,因病情需要使用超过12周时应当向患者说明;④本维莫德在部分患者可产生一过性皮肤刺激,如皮肤瘙痒、灼热感、刺痛感、红斑等,多在用药后2周内发生,大多数无需处理,随用药时间延长可逐渐消失,如果皮肤刺激反应程度较重或用药两周后仍未消退,应暂停使用。
5.2 禁忌证 ①对本维莫德或乳膏中其他任何成分过敏者;②妊娠期、计划妊娠及哺乳期女性;③红皮病型银屑病、泛发性脓疱型银屑病患者。
本维莫德乳膏作为拥有我国完整自主知识产权的国家1类新药,对轻中度寻常性银屑病具有良好疗效和安全性,该药不含激素,且缓解期长,针对银屑病致病的多个环节包括抗炎、调节表皮细胞角化、减少血管新生等发挥作用。本维莫德乳膏为轻、中度斑块型银屑病患者提供了新的外用药物选择。本维莫德乳膏的长期疗效及安全性需要进一步研究。
参与本指导意见制定的专家(按姓氏笔画排序):王刚(第四军医大学西京医院皮肤医院)、史玉玲(上海市皮肤病医院)、孙良丹(安徽医科大学第一附属医院)、杨斌(南方医科大学附属皮肤病医院)、连石(北京大学宣武医院)、张守民(河南省人民医院)、张学军(安徽医科大学第一附属医院/皮肤病研究所)、张建中(北京大学人民医院)、张春雷(北京大学第三医院)、张锡宝(广州医科大学皮肤病研究所)、张福仁(山东省皮肤病医院)、陆前进(中国医学科学院皮肤病医院)、陈爱军(重庆医科大学附属第一医院)、陈翔(中南大学湘雅医院)、郑捷(上海交通大学医学院附属瑞金医院)、郑敏(浙江大学医学院附属第二医院)、耿松梅(西安交通大学第二附属医院)、栗玉珍(哈尔滨医科大学附属第二医院)、顾军(上海市第十人民医院)、徐金华(复旦大学附属华山医院)、高兴华(中国医科大学附属第一医院)、崔勇(中日友好医院)、梁燕华(南方医科大学深圳医院)、曾凡钦(中山大学孙逸仙纪念医院)、路永红(成都市第二人民医院)、蔡林(北京大学人民医院)编写秘书:叶瑞贤(广州医科大学皮肤病研究所)、朱正伟(安徽医科大学第一附属医院)、张耀华(复旦大学附属华山医院)
利益冲突 所有作者均声明不存在利益冲突。所有专家均声明参与本指导意见的制定坚持客观的立场,以专业知识、研究数据和临床经验为依据,所持观点未受到任何企业的影响。本指导意见的制定未接受任何企业、任何形式的赞助。
[1] Bos JD, Spuls PI. Topical treatments in psoriasis: Today and tomorrow [J]. Clin Dermatol, 2008, 26(5): 432-437.
[2] Lowes MA, Bowcock AM, Krueger JG. Pathogenesis and therapy of psoriasis[J].Nature, 2007, 445(7130): 866-873.
[3] 李祥, 张宝兰, 张理涛. 苯烯莫德对银屑病的治疗研究[J]. 中国中西医结合 皮肤性病学杂志, 2017, 16(6): 557-559.
[4] Bissonnette R, Gold LS, Rubenstein DS, et al. Tapinarof in the treatment of psoriasis: A review of the unique mechanism of action of a novel therapeutic AhR modulating agent (TAMA) [J]. J Am Acad Dermatol, 2021, 84(4): 1059-1067.
[5] Quintana FJ, Basso AS, Iglesias AH, et al. Control of Treg and TH17 cell differentiation by the aryl hydrocarbon receptor [J]. Nature, 2008, 453(7191): 65-71.
[6] Stockinger B, Meglio PD, Gialitakis M, et al. The aryl hydrocarbon receptor: multitasking in the immune system [J]. Annu Rev Immunol, 2014, 32(1): 403.
[7] Mascanfroni ID, Takenaka MC, Yeste A, et al. bolic control of type 1 regulatory T cell differentiation by AHR and HIF1-α [J]. Nat Med, 2015, 21(6): 638-646.
[8] Smith SH, Jayawickreme C, Rickard D J, et al. Tapinarof is a natural AhR agonist that resolves skin inflammation in mice and humans[J]. J Invest Dermatol, 2017, 137(10): 2110-2119.
[9] Napolitano M, Patruno C. Aryl hydrocarbon receptor (AhR) a possible target for the treatment of skin disease [J]. Med Hypotheses, 2018, 116: 96-100.
[10]Zheng Y, Danilenko DM, Valdez P, et al. Interleukin-22, a T(H)17 cytokine, mediates IL-23-induced dermal inflammation and acanthosis[J]. Nature, 2007, 445(7128): 648-651.
[11] Nograles KE, Zaba LC, Guttman-Yassky E, et al. Th17 cytokines interleukin (IL)-17 and IL-22 modulate distinct inflammatory and keratinocyte-response pathways [J]. Br J Dermatol, 2008, 159(5): 1092–1102.
[12] Zhu Z, Chen J, Lin Y, et al. Aryl hydrocarbon receptor in cutaneous vascular endothelial cells restricts psoriasis development by negatively regulating neutrophil recruitment [J]. J Invest Dermatol, 2020, 140(6): 1233-1243.
[13] Liu X, Zhang X, Zhang J, et al. Activation of aryl hydrocarbon receptor in Langerhans cells by a microbial bolite of tryptophan negatively regulates skin inflammation [J]. J Dermatol Sci, 2020, 100(3): 192-200.
[14] Furue M, Tsuji G, Mitoma C, et al. Gene regulation of filaggrin and other skin barrier proteins via aryl hydrocarbon receptor [J]. J Dermatol Sci, 2015, 80(2): 83-88.
[15] Johnston A. Resolving inflammation by targeting an ancient innate immune sensor with a bacterial bolite [J]. J Invest Dermatol, 2017, 137(10): 2050-2052.
[16]刘珉宇, 于鹏霞, 赵帅, 等. 苯烯莫德对实验性银屑病的治疗作用[J]. 中国新药与临床杂志, 2016, 35(8): 589-595.
[17] 马晓蕾, 温广东, 赵琰, 等. 苯烯莫德对人外周血单个核细胞增殖、凋亡作用 及对 T 细胞 NF-κB 的调节[J]. 中国皮肤性病学杂志,2014,28(8):785-788,791.